今年もノーベル賞が続々と発表されていますね。
そのうち、ノーベル生理学・医学賞の「細胞が低酸素を検知し応答する仕組みの発見」が気になったので調べてみました。
私たちが酸欠状態になった時に空気を求めるのと同じように、細胞も酸素不足を検知して、さまざまな働きが起こって酸素を取り入れて、酸欠状態を解消しようとします。
ですが、「細胞が酸素不足をどのように検知しているのか」の詳しいメカニズムについてはこれまで謎でした。
その謎を解明したことが今回のノーベル賞受賞につながった功績です。
では、どのようにして細胞は酸素不足を検知しているのでしょうか。
そしてこの功績が、私たちの生活にどのように役に立っているのでしょうか。
Contents
「酸素センサー」低酸素応答の仕組み
今回の受賞の内容は、ノーベル賞の公式ページにコンパクトにまとまっています。
Press release: The Nobel Prize in Physiology or Medicine 2019
肝心の、「酸素の状態をどのように検知しているのか」については次のような図で説明されています(図は上記のプレスリリースより引用)。
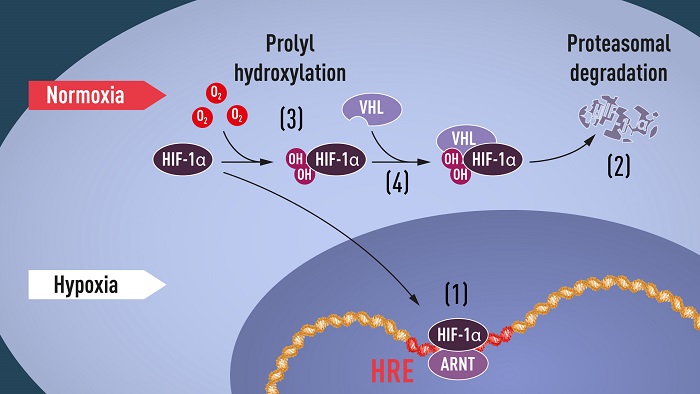
・・・といっても、これだけでは何がなんだか、ですよね。
ということで、ざっくりと説明してみます。
HIF(低酸素誘導因子)の働き
まず、細かなメカニズムは置いておいて、「細胞が酸素不足の状態からどのように酸素を取り入れるのか」をみていきます。
酸素は血液中の赤血球に含まれるヘモグロビンによって、体内に運ばれます。
そのため血液中の赤血球が少なくなると酸素不足になり、逆に酸素不足の状態から回復するには、赤血球を増やせばよい、ということになります。
赤血球を作っているのは骨髄です。
そして、骨髄に対して「赤血球を作れ!」と命令をするのが、腎臓から分泌される「エリスロポエチン」というホルモンです。
なので、エリスロポエチンが多ければ骨髄への「命令」も多くなり、結果として赤血球が多く作られるため、低酸素状態を解消できるというわけですね。
今までの説明が次の図にまとまっています。
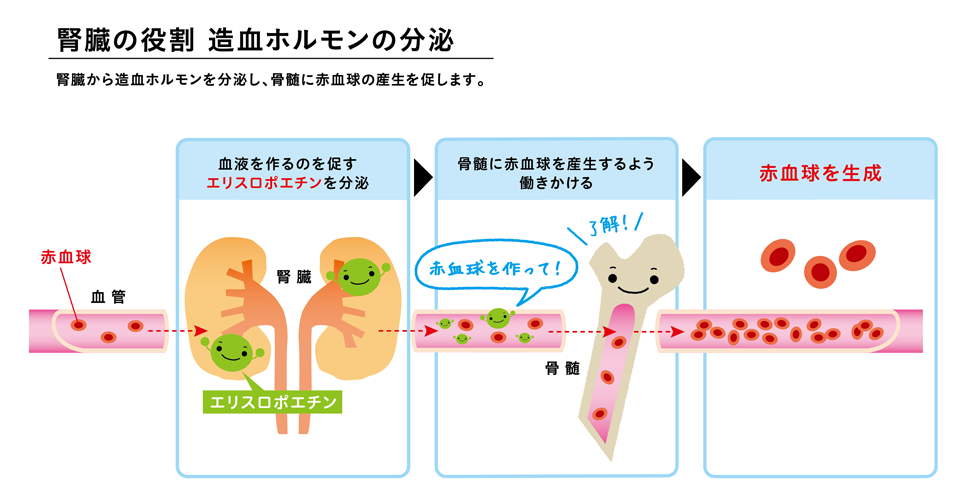
(出典:https://www.frutafruta.com/minagiru/mechanism/)
では、エリスロポエチンは酸素が足りなくなれば腎臓が勝手に分泌するのでしょうか。
実は、通常はエリスロポエチンを産生する細胞は休止状態にあり、ある刺激が加わるとエリスロポエチンの産生をはじめます。
その刺激が、「HIF(Hypoxia-Inducible Factor; 低酸素誘導因子)」というタンパク質によるものです。
HIFは低酸素下で活性化されます。
活性化されると、エリスロポエチンの分泌を促したり、血管を増やすVEGFと呼ばれるタンパク質を活性化したり、体内にさまざまな反応をもたらします。
つまり、このHIFを必要に応じて活性化させたり制御することができれば、病気の治療などにも応用できるのですね。
HIFが低酸素下で活性化する仕組み
HIFは低酸素下で活性化され、通常の酸素状態ではほとんど活性化されません。
この違いは、HIFが低酸素下で増えるというよりも、通常の酸素状態では分解されてしまうため存在できず、低酸素下では分解されないため細胞中に存在し続けることによって生じます。
これまで、この分解のプロセスの詳細は謎のままでした。
今回ノーベル賞を受賞した3者の研究により、低酸素誘導因子HIFが発見され、さらにHIF-1αという種類のHIFの分解プロセスの発見が明らかになりました。
そのプロセスが先ほどの図です。

上のNormoxiaが通常の酸素状態、下のHypoxiaが低酸素状態です。
下の低酸素状態の場合、分解が起こらないのでHIF-1αは活性化され、エリスロポエチンなどさまざまな因子を活性化します。
上の場合、一番右側でProteasomal degradation (プロテアソーム分解)が起き、酵素の一種のプロテアソームによってタンパク質であるHIFは分解されてしまいます。
そのため、通常の酸素状態ではHIF-1αは活性化しません。
プロテアソームはどんなタンパク質でも分解するわけではなく条件があります。
その一つが、「ユビキチン」という別のタンパク質が結合しているかどうか、という条件です。
ですのでHIF-1αが分解されるにはユビキチンが結合している必要があるのですが、ユビキチンが結合するためにはさらにVHLというタンパク質がHIF-1αに結合している必要があることがわかりました。
そしてVHLがHIF-1αに結合するには、HIF-1αが水酸化(-OH基を付加)されている必要があります。
・・・とまあ、ピタゴラスイッチのようにいろんな仕掛けがあって、どこかひとつ「ピース」が欠けていると分解という「ゴール」には至らないということがわかりますね。
このピタゴラスイッチのはじめの「ピース」が、HIF-1αの水酸化です。
低酸素状態であれば、酸素が少ないため確かに水酸化は起こりにくく、分解されにくいということになりますね。
ただ、通常の酸素状態でも、OH基がHIF-1αに結合しなければ分解には至りません。
つまり、通常の酸素状態下でHIF-1αを活性化できるということになります。
この原理、すでに医薬品に応用されていて、日本でも販売間近となっています。
それが、腎性貧血の治療薬「HIF-PH阻害薬」です。
次に、「HIF-PH阻害薬」をもとにして、今回の研究成果の応用についてみていきます。
低酸素応答の応用:HIF-PH阻害薬とは
HIF-PHの仕組みについて、そして従来薬との違いについてみていきます。
HIF-PH阻害薬の仕組み
HIF-PH阻害薬とは、先ほどの反応のはじめの一歩である水酸化反応を阻害する薬です。
HIFはプロリン水酸化酵素(PHD)によって水酸化されます。
そのPHDの働きを阻害することで、HIFへ水酸基が付加されることを防止し、プロテアソームによる分解を防止します。
結果としてHIFを活性化させ、エリスロポエチンなどの因子を活性化します。
これまでの説明が、次の図にまとまっています。
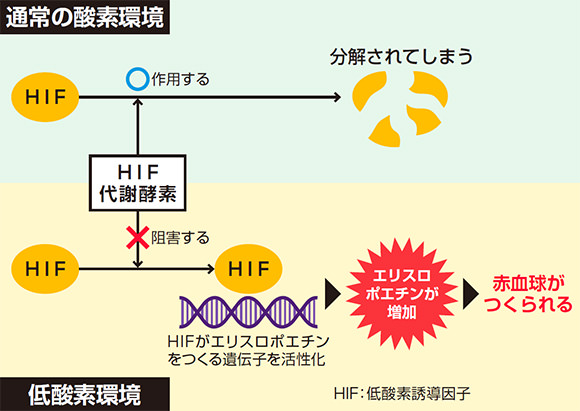
(出典:https://ct-jp.astellas.com/jp/corporate/brand/changing-tomorrow/innovation/article02.html)
エリスロポエチンを活性化すれば、赤血球が産生され貧血状態を改善できます。
そのため腎性貧血治療薬として開発され、2019年10月時点でアステラス製薬の「エベレンゾ」という薬が製造販売承認を取得しています。
ところで「腎性貧血」という言葉、聞き慣れないのではないでしょうか(私は実は今回初めて知りました)。
貧血は、血液中のヘモグロビンが不足している状態のことを指します。
通常、貧血というと「鉄分をとりなさい」と言われますよね。
あれは赤血球に含まれるヘモグロビンを構成する鉄が不足しているためで、このタイプの貧血は「鉄欠乏性貧血」と呼ばれます。
それに対して「腎性貧血」は、赤血球そのものが不足している状態です。
「赤血球を作れ!」と骨髄に命令するのは腎臓で分泌されるホルモン、エリスロポエチンですが、腎臓の機能が弱まればエリスロポエチンの分泌量も低下し、そもそもの赤血球の量が不足することになります。
腎機能低下によりエリスロポエチンの分泌量が低下することで生じる貧血を「腎性貧血」と呼びます。
HIF-PH阻害薬はこの「腎性貧血」を治療する薬になります。
HIF-PH阻害薬とエリスロポエチン製剤の違い
現在、一般に腎性貧血の治療に使用されている薬は「エリスロポエチン製剤」と呼ばれているものです。
「エリスロポエチン製剤」は動物細胞を用いて生産したバイオ医薬品の一種で、合成したエリスロポエチンを静脈注射することで血中ヘモグロビン濃度を上昇させ、貧血を治療しています。
これに対して、HIF-PH阻害薬のひとつ、エベレンゾは経口薬です。
(エベレンゾの添付文書はhttp://www.pmda.go.jp/PmdaSearch/iyakuDetail/ResultDataSetPDF/800126_39990C8F1029_1_02から確認できます)
従来のエリスロポエチン製剤と比較した場合、HIF-PH阻害薬には
- 投与方法が簡便で透析に至らない患者(保存期慢性腎臓病の患者など)への適用が容易
- 室温で長期保存が可能(エリスロポエチン製剤はタンパク質を有効成分とするので冷暗所で保存する必要があった)
- HIF活性化により鉄代謝を調整するヘプシジンにも作用し、より効率よく赤血球が産生できる
などのメリットがあります。
さらに、HIF-PH阻害薬は腎性貧血だけでなく心筋梗塞や脳卒中など、低酸素状態に陥っている他の臓器の障害の進行を遅らせる効果も期待されています。
今後腎性貧血以外でも、HIF-PH阻害薬の適用疾患が増えてくるかもしれません。
まとめ
今年(2019年)のノーベル生理学・医学賞を受賞した「細胞が低酸素を検知し応答する仕組みの発見」と、その仕組みを応用した薬剤についてざっくりとみてきました。
低酸素誘導因子HIFが活性化されることで、エリスロポエチンの分泌が促進されます。
それによって赤血球が産生され、低酸素状態が解消に向かいます。
通常の酸素状態では、まずHIFが水酸化され、水酸化されたHIFにVHLが結合し、それを標識にしてユビキチンが結合することでプロテアソームにより分解されます。
HIFの水酸化を阻害することで分解を阻害し、エリスロポエチンの分泌を促進させるHIF-PH阻害薬がもうすぐ日本でも販売となります。
今後、HIFにまつわる研究と臨床試験が進めば、さらにHIFを利用した薬剤の適用は増えてくるでしょう。
主な参考文献: