新型コロナウイルスの治療薬やワクチンの試験結果などのニュースを、最近よく目にしますね。
特に、アメリカ・モデルナ社など複数社が開発中の「mRNAワクチン」については、第1相試験の結果は概ね良好で、モデルナ社のmRNAワクチンは、早くも第3相試験に入るというプレスリリースがされていました(モデルナ社ウェブサイトより)。
しかし、このmRNAワクチンってそもそもどんなワクチンなのでしょうか。
少し調べてみますと、まだ世界で承認されたことのない種類のワクチンのようです。
果たして、mRNAワクチンは「新型コロナウイルスワクチン」として私たちの前に登場するのでしょうか。
新型コロナウイルスの構造とウイルス抗原
ワクチンの話をする前に、少しだけ新型コロナウイルスについて復習しておきます。
新型コロナウイルス感染症(COVID-19)は、SARS-CoV-2と呼ばれる新型コロナウイルスに感染することによって起こります。
SARS-CoV-2の構造は次のようになっています(左は電子顕微鏡写真)。
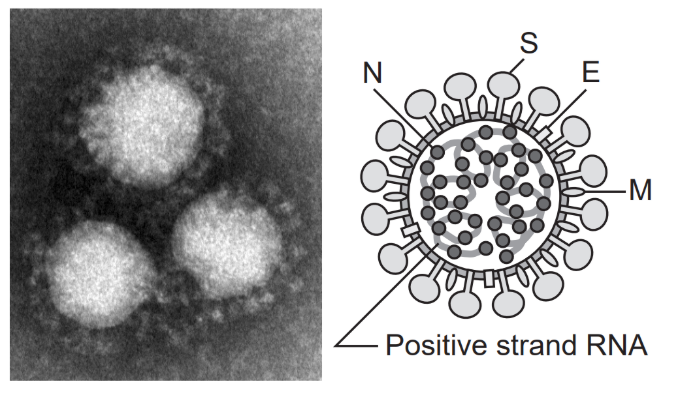
(出典:https://www.niid.go.jp/niid/ja/kansennohanashi/9303-coronavirus.html)
エンベロープ外側に突き出ているスパイクタンパク質(上記図の「S」)が宿主細胞受容体(ACE2受容体)と結合して、細胞内に進入します。
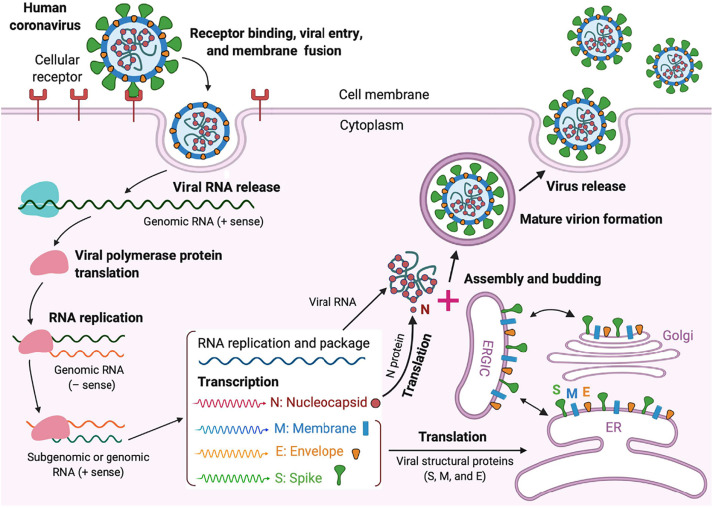
(出典:https://www.sciencedirect.com/science/article/pii/S0141813020338691)
SARS-CoV-2は一本鎖RNA+鎖ウイルスに分類されます。
ゲノムがRNAなので、細胞質で宿主細胞のリボソームを拝借してウイルスゲノムとタンパク質の複製に必要なRNA依存性RNAポリメラーゼをまず生成し、その後、各パーツの複製と組立を行い、出芽します。
SARS-CoV-2に対しては、主に、細胞側の受容体と結合するスパイクタンパク質を抗原としたウイルスの開発が進んでいます。
mRNAワクチンの優位性
ワクチンは、その形態、製造方法、投与方法などにより様々に分類されます。
ここでは、従来の「外部から抗原を投与するワクチン」と、「体内で抗原が発現するワクチン」に大別しました。
新型コロナウイルスワクチンとして開発されていないもの(細胞毒素であるトキソイドなど)も含んでいます。
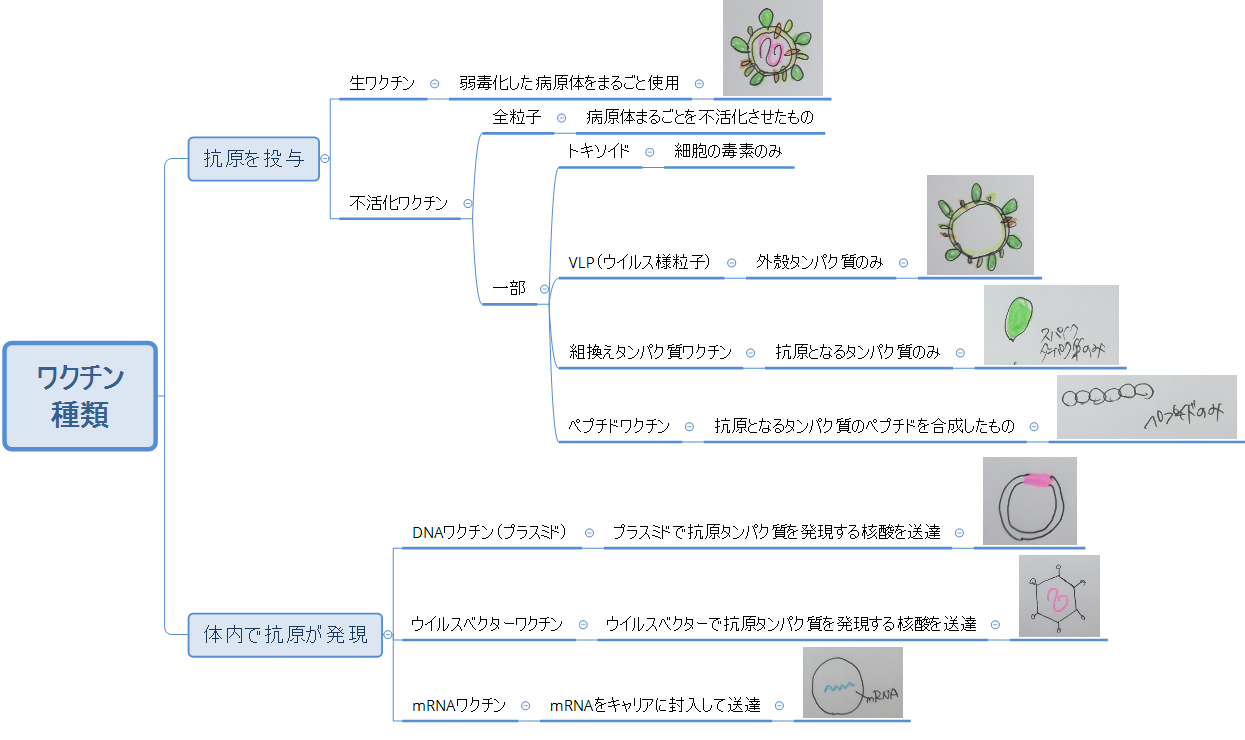
安全性と免疫原性のバランス
「抗原を投与」のグループは大きく「生ワクチン」と「不活化ワクチン」に分けられます。生ワクチンは必要な免疫原性(免疫応答を引き起こす能力)を維持しつつ病原性を抑えた病原体そのものを投与するワクチンで、「実際に病原体が体内に入った」状態と一番近いので、ワクチンとしての効果も優れています。
ただ、弱毒化したとはいえ病原体そのものであるので安全性の懸念があります。
不活化ワクチンは、病原体の病原性を完全になくしたワクチンですので安全性は高いのですが、その分生ワクチンと比較すると免疫原性に劣ります。
そのため、一般にアジュバント(免疫原性を高めるための物質)を別途添加する必要があります。これも副作用などの懸念があります。
安全性と免疫原性はトレードオフの関係にあるといえますね。
「体内で抗原が発現」のグループは、抗原(新型コロナウイルスワクチンの場合はスパイクタンパク質など)を発現する配列情報を持った核酸をプラスミド、ベクター、またはmRNAの形で投与することで、体内でその抗原が産生され、免疫が誘導されるという仕組みです。
ウイルスベクターワクチンについては、エボラウイルス用ワクチンとして中国と欧州で承認例があるのみで、プラスミドを用いたDNAワクチン、そしてmRNAワクチンはまだ承認例はありません。
この形態の場合、生ワクチンを投与した場合と同様、液性免疫(抗体による免疫)と細胞性免疫(キラーT細胞などによる抗原への直接攻撃、自然免疫系の強化)のいずれも誘導できるとされています。
細胞性免疫は、新型コロナウイルスワクチンとしても開発が進んでいる組換えタンパク質ワクチンなどの他の形態では引き出せないとされているので、この点ではDNAワクチン、mRNAワクチンは魅力があるといえそうです。
DNA挿入変異のリスクなし
mRNAワクチンにはもう一点、安全性に関して有利な点があります。
それは宿主の核ゲノムに挿入されることのないRNAである、ということです。
ウイルス複製手段として宿主のゲノムを用いるベクターでは、宿主の染色体に組み込まれて目的のタンパク質を産生する遺伝子を発現させます。
この場合、意図しない場所にウイルスゲノムが挿入された場合などに、宿主の染色体上の他の遺伝子の発現に影響を与え、白血病発症などのがん化のリスクがあります。
mRNAワクチンは、細胞質でmRNAからそのまま目的タンパク質が翻訳されます。
この挿入変異リスクがないことも、mRNAワクチンは安全性が高いと言われる一つの理由です。
パンデミックに対応できる製造方法
製造方法から見ても、DNAワクチン、特にmRNAワクチンには優位性があります。
従来のワクチンは、鶏卵法(鶏の卵の中でウイルスを増殖させる)、細胞培養法(動植物細胞、昆虫細胞などで培養)という手法が用いられています。
培養、そしてその後の精製工程と、工数がかかります。

(出典:https://www.jiu.ac.jp/features/detail/id=6587)
DNAワクチンも培養・精製工程が必要となります。
それに対して、mRNAワクチンは、抗原の配列がわかればワクチンの設計が容易です。
つまり、抗原が変異した場合であっても、それに対応する配列に変更することで素早くワクチンを製造することができます。
これは、今回の新型コロナウイルスのように、パンデミック時や変異しやすいウイルスに対するワクチンとしては大きなメリットです。
新型コロナウイルスに対する多くのワクチンが開発中ですが、特にmRNAワクチンの治験が先行しているのは開発・製造のしやすさもあると考えられます。
mRNAワクチンの課題
このように、ワクチンとして魅力的なmRNAワクチンですが、1990年代から着想があったにもかかわらずこれまで実例がないのは、やはり大きな課題が存在しているからです。
主な課題としては、下記の2点が挙げられます。
- mRNAは体内で非常に不安定であること
- mRNA自体が免疫反応を誘発すること
体内にはリボヌクレアーゼ(RNA分解酵素)が存在しており、RNAはそのままでは消化されてしまいます。
そのため、mRNAワクチンは脂質ナノ粒子などのキャリアに封入して送達するように設計がなされています。
そして、mRNA自体に免疫原性があるため、体内に入ると異物とみなされて自然免疫系の免疫応答を誘発してします。
さらには、現在キャリアとして主に使用されている脂質ナノ粒子も炎症反応を惹起しやすいとされており、DDS(ドラッグデリバリーシステム)技術がmRNAワクチンの成功の鍵のひとつであるといえそうです。
実際、ナノ医療イノベーションセンター(iCONM)と東京都医学総合研究所(TMIMS)が開発中の新型コロナウイルス用のmRNAワクチンは、キャリアとして高分子ミセルを採用することで、mRNAが安全に送達されているように設計されています。
(iCONMと東京都医学総合研究所、新型コロナにmRNAベースのワクチンを開発へ(日経バイオテク)に詳細が掲載されています)
また、上記の記事で開発中のmRNAはとてもユニークで、部分的に2本鎖になっている「部分2本鎖mRNA」を採用しています。
この形が完全な1本鎖または2本鎖RNAと比較して、強い免疫応答と高い翻訳効率を兼ね備えた理想型であったようです。
また、ドイツ・CureVec社が開発中のmRNAワクチンは、非翻訳領域(UTR)やタンパク質へ翻訳されるオープンリーディングフレーム(ORF)をカスタマイズして、タンパク質への翻訳効率を最適化させています(記事はこちら)。
ここまでの調査で、mRNAワクチン技術としては、DDS技術、免疫応答と翻訳効率を向上させる技術、mRNA自体の免疫原性を低下させる技術が必要な技術であるということがわかってきました。
おそらく、mRNAワクチンの関連特許もこのあたりをどう克服していくかという話なのではないか、と予想しつつ、次はmRNA関連の明細書を読んでいこうと思います。
まとめ
数ある開発中の新型コロナウイルスワクチンの中で、mRNAワクチンについて少し詳しく調べてみました。
mRNAワクチンは、安全性が高く、細胞性免疫も誘発でき、ワクチン設計・製造が他の方法に比べて容易であることから、次世代のワクチンとして注目されています。
安全で確実な送達のための課題は残されていますが、今後の治験結果が良好であれば、新型コロナウイルスワクチンとして承認される可能性も十分あるのではないかとみています。
主な参考文献